Ein Magenkarzinom tritt häufig im mittleren und späteren Erwachsenenalter auf. In über 90% der malignen Tumoren des Magens handelt es sich um Adenokarzinome, lokalisierte gastrische Lymphome und Leiomyosarkome kommen seltener vor. Mittels MRI können verschiedene morphologische Formen des Adenokarzinoms differenziert werden. CT hat für Diagnosezwecke kaum eine Bedeutung, wird aber oft für das Tumorstaging eingesetzt.
Zahlreiche pathologische Veränderungen als Ursache der Dysphagie wurden im Rahmen dieser Serie in der Hausarzt Praxis 2022 bereits besprochen. Neben der Lokalisation von Raumforderungen mit konsekutiven Schluckstörungen im Bereich des Hypopharynx, Larynx und Ösophagus sowie von extern die Passage der Nahrung behindernden Prozessen steht im vorliegenden Beitrag das Magenkarzinom im Fokus.
Die Inzidenz und die Letalität des Magenkarzinoms haben in den letzten Jahren abgenommen. Die Rate der jährlichen Neuerkrankungen lag in Deutschland 2007 bei 19 400, der Anteil der Männer bei 11 200 [7]. 85% der Malignome waren Adenokarzinome. Obwohl im mittleren Abschnitt der Verdauungsorgane gelegen, können die tumorösen Veränderungen des Magens durchaus eine die Passage des Speisebreis behindernde Wirkung und eine Dysphagie entfalten. In Übersicht 1 sind die unterschiedlichen Symptome [1], die vom Magenkarzinom ausgehen können, aufgeführt.

Im Initialstadium des Magenkarzinoms finden sich keine oder nur geringe, uncharakteristische Beschwerden. Diese werden oft nicht beachtet oder als harmlose Nahrungsunverträglichkeiten fehlgedeutet. Häufig ist das Magenkarzinom im mittleren und späteren Erwachsenenalter zu beobachten [5]. Die superfizielle Form ist eher selten. Chronische Vorerkrankungen können die Entstehung des Malignoms begünstigen [2], wie z.B. die perniziöse Anämie [3] und der Morbus Menetrier [4]. Dabei handelt es sich um eine atrophische Gastritis mit megaloblastärer Anämie bzw. Vitamin-B12-Mangelanämie. Die Menetrier’sche Erkrankung ist eine Riesenfaltengastritis. Gelegentlich kommen Magenulcera vor. Die Diagnose wird in beiden Fällen histologisch gestellt.
Das Adenokarzinom ist der am häufigsten vorkommende Gewebstyp [6]. In diesem Zusammenhang sind auch Infektionen mit Helicobacter pylori als begünstigender Faktor nachgewiesen worden.
Röntgenaufnahmen spielen in der Diagnostik des Magenkarzinoms keine Rolle. Früher war die Doppelkontrastuntersuchung des Magens in Hypotonie die primäre bildgebende Untersuchung, um tumoröse Prozesse und funktionelle Störungen des Magens nachzuweisen. Nach Einführung der Endoskopie spielt diese bildgebende Methode keine Rolle mehr. Prinzipiell gilt die Endoskopie als das diagnostische Tool der Wahl.
Sonografisch sind unter optimalen Schallbedingen nach Flüssigkeitsfüllung des Magens Raumforderungen der Magenwand zu identifizieren. Grosse und konstante Kokarden sind suspekt und die sonographisch kontrollierte Palpation zeigt den Tumor wenig verformbar [9].
Computertomografische Untersuchungen werden primär zur Diagnostik des Magenkarzinoms selten angefordert. Im Staging hat sich die Methode bewährt, um wandüberschreitendes Tumorwachstum, Lymphknoten- oder Organmetastasen zu verifizieren. Beim oral mit Wasser gut gefüllten Magen sind Wandverdickungen mit mehr als 4 mm tumorsuspekt, nodulär oder irregulär konturiert [8].
Kernspintomografisch können vier morphologische Formen des Adenokarzinoms differenziert werden(Übersicht 2). Die Tumoren sind isointens zur Magenwand in T1w, leicht hyperintens in T2w und weisen ein deutliches Signalenhancement nach Kontrastmittelgabe auf [10].

Fallbeispiele
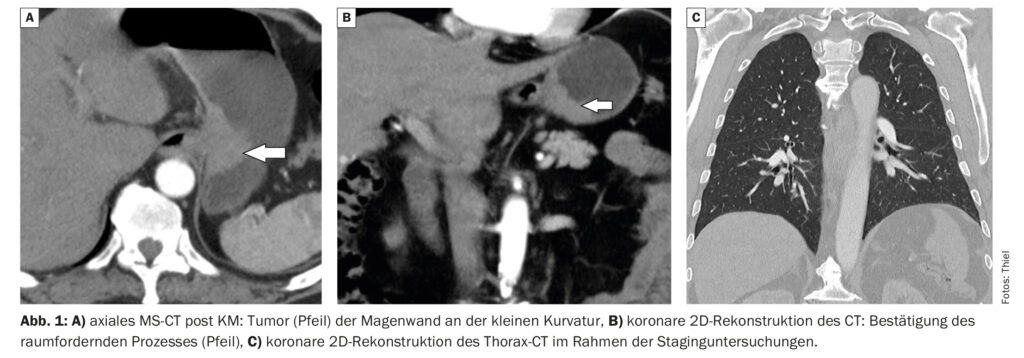
Das erste Fallbeispiel zeigt ein histologisch gesichertes Adenokarzinom des Magens eines 72-jährigen Patienten (Abb. 1A und B) mit Oberbauchschmerzen, Übelkeit, Gewichtsverlust und Appetitlosigkeit. Im Rahmen des Stagings konnten pulmonale Filiae ausgeschlossen werden (Abb. 1C).
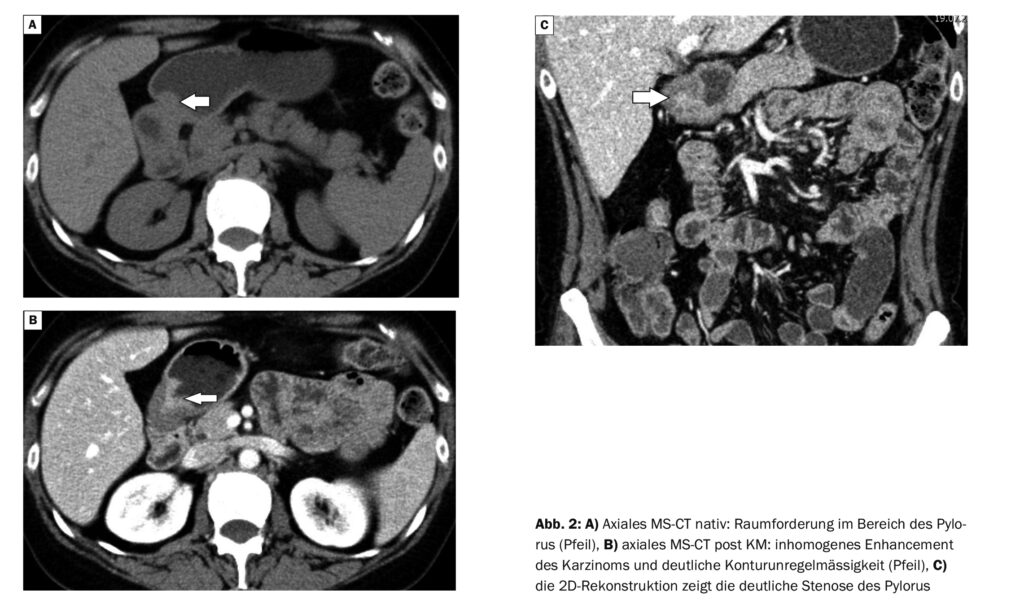
Im Fallbeispiel 2 wurde im CT ein Magenkarzinom im distalen Korpus und Pylorus detektiert (Abb. 2A bis C). Die 51-jährige Patientin war mit Mittelbauchschmerzen, Abgeschlagenheit, Müdigkeit und Erbrechen auffällig. Histologisch wurde ebenfalls ein Magenkarzinom gesichert.
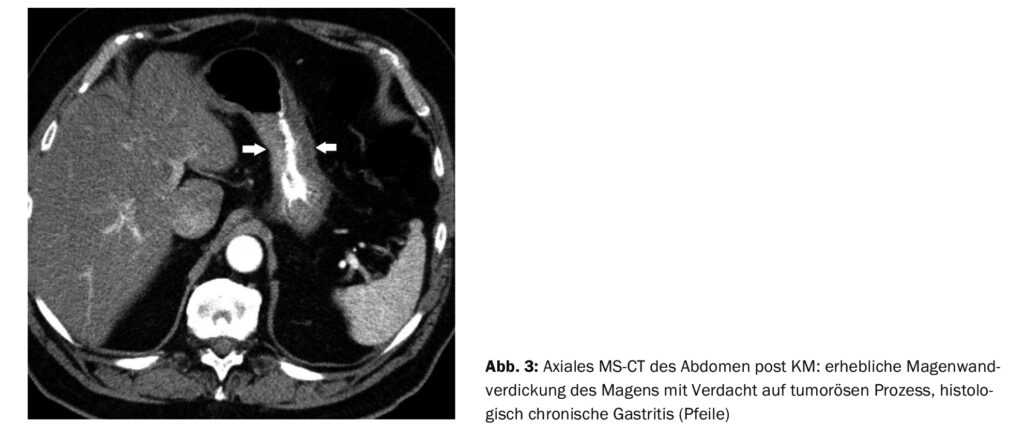
Fallbeispiel 3 zeigt, dass die CT zwar eine grosse Sensitivität, aber geringere Spezifität in der Diagnostik der Magenschleimhauttumoren hat. Im Fall des 72-jährigen Patienten mit Prostata-Karzinom war im Rahmen des Stagings auch eine auffällige Magenwandverdickung zu sehen (Abb. 3), die sich histologisch aber einer chronischen Gastritis zuordnen liess.
Take-Home-Messages
- Das Adenokarzinom ist der häufigste maligne Tumor des Magens.
- Die Inzidenz ist in den letzten Jahren rückläufig.
- Bei Männern ist das Malignom etwas häufiger zu finden als bei Frauen,
vorrangig im mittleren Lebensabschnitt. - Diagnostische Methode der Wahl ist die Endoskopie, die auch eine
histologische Sicherung ermöglicht. - Die Schnittbildverfahren haben einen hohen Stellenwert im Staging.
Literatur:
- Ajani JA, et al.: Gastric adenocarcinoma. Nat Rev Dis Primers 2017; 3: 17036.
- Arfaoui D, et al.: Epidemiologic profile of gastric carcinoma: study of 140 cases. Tunis Med 2006; 84(5): 301–304.
- Burgener FA, et al.: Differenzialdiagnostik in der MRT. Georg Thieme Verlag: Stuttgart, New York, 2002; 555.
- Dietel M, Suttorp N, Zeitz M (Hrsg.): Harrisons Innere Medizin. Band 1. 17. Auflage. ABW Wissenschaftsverlag GmbH: Berlin 2009; 709.
- DocCheck Flexikon, https://flexikon.doccheck.com/de/Perniziöse_
Anämie, (letzter Abruf 14.12.2022) - Medicoconsult, www.medicoconsult.de/morbus_menetrier, (letzter Abruf 141.12.2022)
- Prokop M, Galanski M (Eds): Computed Tomography of the Body. Georg Thieme Verlag: Stuttgart, New York 2003; 559–561.
- Rebai W, et al.: Early gastric adenocarcinoma. Tunis Med 2010: 88(1): 1–4.
- Stahl M: Magenkrebs – Symptome, www.krebsgesellschaft.de/basis-informationen-krebs-allgemeine-informationen.html,
(letzter Abruf 14.12.2022) - Struve C: Sonographie des Abdomens. 4., überarbeitete und erweiterte Auflage. Urban & Schwarzenberg: München, Wien, Baltimore 1991; 87.
HAUSARZT PRAXIS 2023: 18(1): 40–42



