Neben der Operation und Chemotherapie ist die Erhaltungstherapie die dritte Säule der Behandlung des Ovarialkarzinoms in einem fortgeschrittenen Stadium. Primär werden PARP-Inhibitoren nach einer Chemotherapie eingesetzt. Ziel dabei ist, den Effekt beziehungsweise die Tumorkontrolle, die mithilfe der Chemotherapie erreicht werden konnte, möglichst lange aufrecht zu erhalten oder zu stabilisieren.
Die Therapie des Ovarialkarzinoms hat sich in den letzten Jahren stark verändert und grosse zulassungsrelevante Studien sowie regulatorische Meilensteine in der Erstlinien-Erhaltungstherapie hervorgebracht. Beginnend im Jahr 2011 mit der ICON-Studie über Bevacizumab [2], folgte 2018 die SOLO1-Studie über Olaparib [3]. Kurz darauf im Jahr 2019 wurden die PRIMA-Studie über Niraparib [4], die PAOLA-1-Studie über Olaparib plus Bevacizumab [5] und die VELIA-Studie über Veliparib plus PLT-basierter Chemotherapie [6] veröffentlicht.
Die Entwicklung der First-Line-Erhaltungstherapie
Die Behandlung des Ovarialkarzinoms besteht aus mehreren Therapien, die gut ineinandergreifen müssen, um für die Patientin einen optimalen Nutzen zu erreichen. So ist eine komplette R0-Sektion entscheidend um die signifikante Überlebenschance von Patientinnen zu erhöhen, da sie die Tumorlast für die nachfolgende Chemotherapie senkt [7]. Darüber hinaus besteht die Möglichkeit einer neoadjuvanten Chemotherapie bei Ovarialkarzinomen im Stadium IIIC oder IV [8]. Nach vorrangegangener 6 Zyklen platinbasierter Chemotherapie kann die Gabe von PARP Inhibitoren erfolgen. Mit der Zulassung von PARP Inhibitoren ist ein weiterer bedeutsamer Fortschritt erzielt worden, da sie das progressionsfreie Überleben beim fortgeschrittenen Ovarialkarzinom statistisch signifikant verlängern und zudem das Rezidivrisiko bei Patientinnen mit fortgeschrittenem Ovarialkarzinom um 60-85% verringern [9].
Erhaltungstherapie mit PARP Inhibitoren
PARP-Inhibitoren sind Hemmstoffe des Enzyms Poly-ADP-Ribose-Polymerase (PARP) und verhindern, dass Krebszellen einen durch Zytostatika induzierten DNA-Schaden reparieren. Wenn die Replikationsgabeln auf das PARP-DNA-Addukt stossen, kommt es zu einem Doppelstrangbruch. In normalen Körperzellen können Doppelstrangbrüche durch homologe Rekombination repariert werden. Bei Krebszellen, denen Komponenten der homologen Rekombinationsreparatur (HRR) fehlen, können Doppelstrangbrüche nicht suffizient repariert werden. Alternativ werden von der Zelle fehleranfällige Reparaturwege wie die nicht-homologe Endverknüpfung (NHEJ) angestossen. Das führt zu einer erhöhten genomischen Instabilität der Tumorzelle. Nach mehreren Replikationsrunden wird die genomische Instabilität so gross, dass die Zelle in die Apoptose getrieben wird. Klinisch kommt es zur Regression des Tumors. Vor allem bei BRCA mutierten Tumoren ist die homologe Rekombinationsreparatur defekt, was die Chance zur Regression des Tumors nochmal erhöht [10].
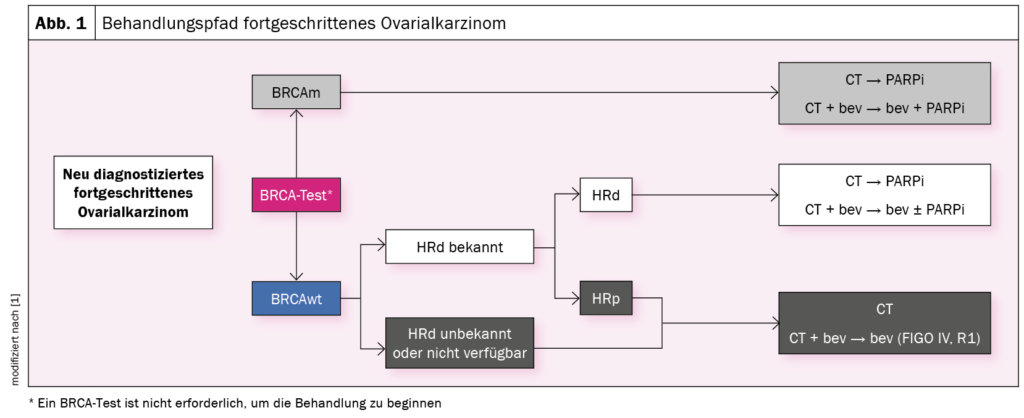
Biomarker basierter Algorithmus kann bei Behandlungsentscheidungen helfen
Auf die Diagnose fortgeschrittenes Ovarialkarzinom sollte eine BRCA Testung folgen, da die genetische Testung einen signifikanten Einfluss auf die Erstlinientherapie hat. Sind die Krebszellen BRCA-mutiert (BRCAm) besteht die Option einer Chemotherapie plus Erhaltungstherapie, eventuell kombiniert mit Bevacizumab. Sind die Krebszellen nicht BRCA-mutiert (BRCAwt) sollte eine HRd-Testung erfolgen. Liegt eine HRd-Mutation vor (HRd) kann auch in diesem Fall eine Chemotherpie plus Erhaltungstherapie erfolgen. Liegt keine HRd-Mutation vor (HRp) erfolgt lediglich die Chemotherapie, eventuell kombiniert mit Bevacizumab (Abb. 1) [1]. In der Regel sind Ovarialkarzinome zu 25% BRCA und HRd-mutiert, weitere 25% sind nur HRd-mutiert und die restlichen 50% sind weder BRCA noch HRd-mutiert. Liegt sowohl eine BRCA als auch eine HRd-Mutation vor, kann also eine Erhaltungstherapie mit Niraparib, Olaparib oder Olaparib plus Bevacizumab erfolgen. Zusätzlich besteht bei einer HRd-Mutation die Möglichkeit Niraparib oder Olaparib plus Bevacizumab zu verabreichen. Liegt weder eine BRCA oder HRd-Mutation des Ovarialkarzinoms vor sind PARP-Inhibitoren in der Schweiz bisher nicht zugelassen.
In die Entscheidung für eine Behandlung mit PARP Inhibitoren fliessen neben der genetischen Testung noch weitere Aspekte. Neben Patientenmerkmalen wie Begleiterkrankungen, dem Gesamtbehandlungsalgorithmus, der Patientenpräferenz, oder der Lebensqualität, fliessen auch Krankheitsmerkmale, wie klinische Merkmale oder molekulare Eigenschaften in die Entscheidung. Darüber hinaus wird die Entscheidung auch von den Arzneimitteleigenschaften, wie Sicherheit und Wirksamkeit, einfache Verwaltung, individuelle Dosierung oder Wechselwirkungen mit anderen Medikamenten, beeinflusst. Und auch die Zugänglichkeit von genetischen BRCA- und HRd-Tests sowie Zulassungen und Indikationen, spielen eine entscheidende Rolle [11-14].
Nebenwirkungen und Abbruchrate bei Monotherapien niedriger
Zu den häufigsten Nebenwirkungen bei der Erhaltungstherapie zählt die Thrombozytopenie, gastrointestinale Symptome und Müdigkeit. PARP-Studien zeigen jedoch, dass die Abbruchrate bei Niraparib und Olaparib lediglich bei 12% liegt und bei einem Placebo kombiniert mit Bevacizumab sogar nur bei 6%. Allein bei der Kombinationstherapie von Olaparib in Kombination mit Bevacizumab liegt die Abbruchrat mit 20% etwas höher, da es bei der Kombination mehrerer Therapien auch zu einer Häufung der Nebenwirkungen kommen kann [3-5].
Quelle:
1. PD Dr. med. Sara Imboden: PARP inhibitors: Optimizing Therapy in Advanced Ovarian Cancer. Vortrag Jahreskongress gynécologie suisse 2021, 24.06.2021.
2. Burger, R. et al.: Incorporation of Bevacizumab in the Primary Treatment of Ovarian Cancer. N Engl J Med 2011; doi: 10.1056/NEJMoa1104390.
3. Moore, K. et al.: Maintenance Olaparib in Patients with Newly Diagnosed Advanced Ovarian Cancer. N Engl J Med 2018; doi: 10.1056/NEJMoa1810858.
4. González-Martín, A. et al.: Niraparib in Patients with Newly Diagnosed Advanced Ovarian Cancer. N Engl J Med 2019; doi: 10.1056/NEJMoa1910962.
5. Ray-Coquard, I. et al.: Olaparib plus Bevacizumab as First-Line Maintenance in Ovarian Cancer. N Engl J Med 2019; doi: 10.1056/NEJMoa1911361.
6. Coleman, R. et al: Veliparib with First-Line Chemotherapy and as Maintenance Therapy in Ovarian Cancer. N Engl J Med 2019; doi: 10.1056/NEJMoa1909707.
7. du Bois, A. et al.: Role of surgical outcome as prognostic factor in advanced epithelial ovarian cancer: a combined exploratory analysis of 3 prospectively randomized phase 3 multicenter trials: by the Arbeitsgemeinschaft Gynaekologische Onkologie Studiengruppe Ovarialkarzinom (AGO-OVAR) and the Groupe d’Investigateurs Nationaux Pour les Etudes des Cancers de l’Ovaire (GINECO). Cancer 2009; doi: 10.1002/cncr.24149.
8. Vergote, I. et al.: Neoadjuvant chemotherapy or primary surgery in stage IIIC or IV ovarian cancer. N Engl J Med 2010; doi: 10.1056/NEJMoa0908806.
9. Cortez, A. et al.: Advances in ovarian cancer therapy. Cancer Chemother Pharmacol 2018; doi: 10.1007/s00280-017-3501-8.
10. Chelariu-Raicu, A. et al.: Phase Ib/II study of weekly topotecan and daily gefitinib in patients with platinum resistant ovarian, peritoneal, or fallopian tube cancer. Int J Gynecol Cancer 2020; doi: 10.1136/ijgc-2020-001863.
11. Buechel, M. et al.: Treatment of patients with recurrent epithelial ovarian cancer for whom platinum is still an option. Ann Oncol 2019; doi: 10.1093/annonc/mdz104.
12. Mirza, M. et al.: The forefront of ovarian cancer therapy: update on PARP inhibitors. Ann Oncol 2020; doi: 10.1016/j.annonc.2020.06.004.
13. O’Cearbhaill, M.: Using PARP Inhibitors in Advanced Ovarian Cancer. Oncology (Williston Park) 2018; doi: PMC6662180.
14. Havrilesky, L. et al.: Cost-effectiveness analysis comparing “PARP inhibitors-for-all” to the biomarker-directed use of PARP inhibitor maintenance therapy for newly diagnosed advanced stage ovarian cancer. Gynecologic Oncology 2020; doi: 10.1016/j.ygyno.2020.08.003.
Isabell Bemfert